新版药品管理法主线:MAH制度全面实施,CRO、CMO/CDMO行业将迎爆发风口 |
您所在的位置:网站首页 › 医药cro cmo › 新版药品管理法主线:MAH制度全面实施,CRO、CMO/CDMO行业将迎爆发风口 |
新版药品管理法主线:MAH制度全面实施,CRO、CMO/CDMO行业将迎爆发风口
|
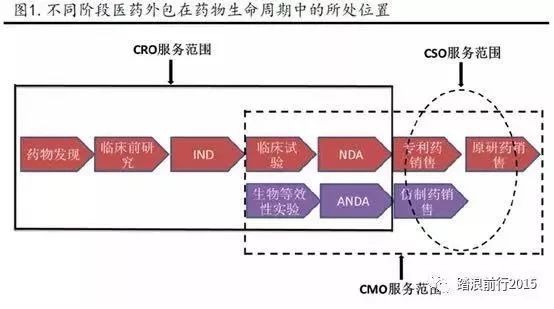
关于MAH制度的优势 鼓励药物创新、提升竞争能力 实行上市许可持有人制度,允许药物研发机构作为药品注册的申请人提交药物临床试验申请、药品上市申请,取得药品批准文号后,成为上市许可持有人。这意味着药物研发机构,可以上市许可持有人的身份享有技术创新所带来的最终市场收益,这将激发更多的研发机构和科研人员从事新药创制。 优化资源配置、促进产业集中 上市许可持有人制度具有注册申请放开、委托生产放开、许可转让放开、集团持有放开等许多制度红利。全面实施这一制度,市场竞争、优胜劣汰的活力将进一步迸发,创新集聚、产业集中的步伐将进一步加快,质量变革效率变革动力变革的高质量发展将进一步夯实。 落实主体责任、强化全程管理 长期以来,研制、生产、流通、使用、进口环节的药品质量风险由不同主体把关,系统完备、环环相扣的闭环管理体系尚未完全形成。上市许可持有人制度实行后,上市许可持有人作为药品的“出品人”,是药品安全、有效和质量稳定的第一责任人,对药品临床前研究、临床试验、生产制造、经销配送、不良反应监测、药物警戒等承担管理责任,这有利于上市许可持有人全面加强自身质量管理体系建设,并延伸对合作方质量管理体系的审查,进而强化药品全生命周期质量体系,有效控制药品质量安全风险。 促进管理创新、实现管理升级 无论是对监管部门,还是对药品企业,实行上市许可持有人制度均涉及管理理念、制度、机制、方式、战略的创新。从企业的角度看,上市许可持有人需要建立一套新的药品质量保证体系,以保障药品质量风险责任的全面落实。从政府的角度看,需要创新药品监管方式方法,以进一步提高监管质量和监管效能。 随着新修订的《药品管理法》的颁布出台,药品上市许可持有人制度(MAH)体现出让医药市场要素灵活的流动,不具备药品经营生产和经营资质的机构和个人只要有创新能力,都可以持有药品批件,通过委托授权其他生产企业生产或销售经营企业来进行销售,而不是过去将批文绑定在生产企业,这势必将促进医药服务外包的三种形式上游发研发外包CRO、生产外包CMO、营销外包CSO的爆发式增长。
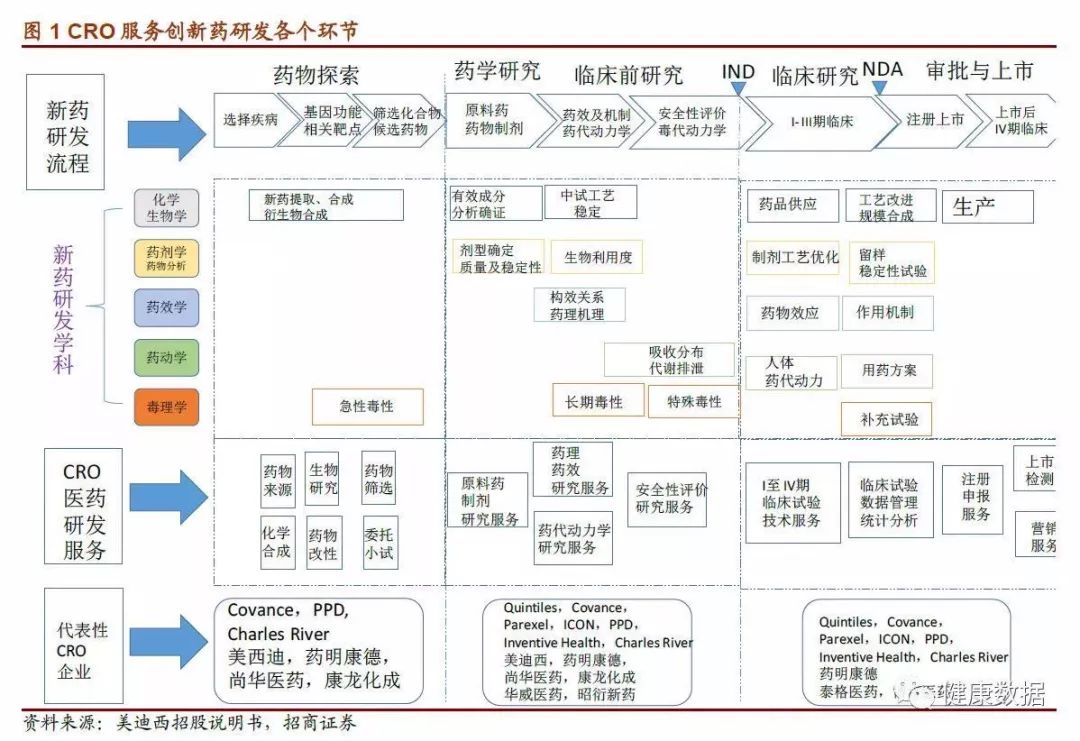
根据国际著名的市场研究公司Frost & Sullivan研究,2018年全球CRO市场规模约487亿美元,中国CRO市场规模约111亿美元。根据Frost&Sullivan报告预测,未来制药企业在研发成本提升与专利悬崖的双重挤压下,聘用外部CRO的意愿会进一步增强。全球CRO市场有望保持10.5%左右的增速较快增长,预计2022年全球CRO市场规模将达到727亿美元,中国整个CRO市场规模将近150亿美元。 CRO(Contract Research Organization)是"合同研发组织",一般称之为"研发外包服务"。出现于上世纪80年代,一种学术性或商业性的科学机构。申办者可委托其执行临床试验中的某些工作和任务,此种委托必须作出书面规定,其目的是通过合同形式向制药企业提供新药临床研究服务的专业公司。 CRO的工作可以覆盖新药研发及试验的各个环节,按照覆盖的药物研发环节的不同,CRO又可以分为临床前CRO和临床CRO。
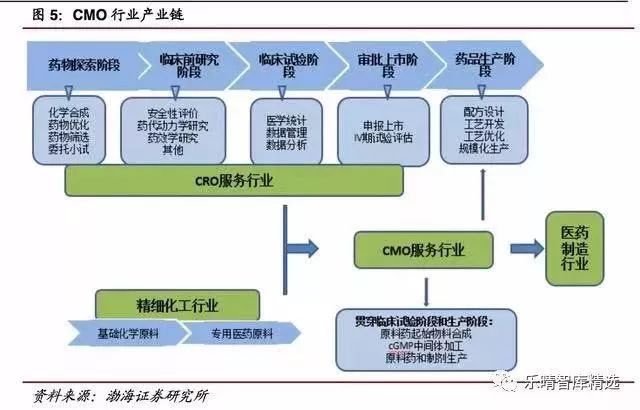
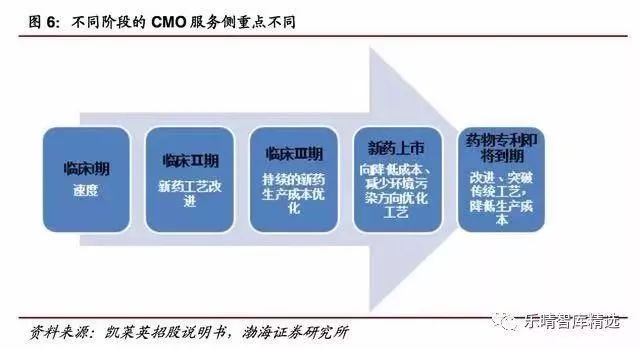
CRO 企业深度介入创新药产业链,节省药企研发时间和研发支出,提升制药企业的研发效率。统计数据显示,企业选择CRO 服务,研发时间可以节省约30%。 药物开发是一项高技术、高投入、高风险、长周期的复杂系统工程,根据外包服务阶段的不同可以划分为CRO和CMO。随着CMO市场趋于成熟,还衍生出定制生产(CDMO)、产研结合(CRO+CMO/CDMO)等多种模式。近年,全球CMO市场平均增速为13.03%,欧美CMO行业起步较早,现阶段产业构架已趋于成熟,而新兴市场国家的CMO行业由于各项机制逐渐健全、成本相对低廉等因素迅速崛起,其中我国CMO行业以18.3%的增速快速发展。据BusinessInsights统计,2021年全球CMO行业将达到1025亿美元规模,中国整个CMO市场将到达626亿元。 CMO是医药生产外包服务,是以合同定制形式为制药企业提供临床用药、中间体制造、原料药生产、制剂生产以及包装等专业服务的企业。 CMO按服务类型主要划分为API(ActivePharmaceuticalIngredient,原料药和中间体)和DP(FinishedDosageForms,最终剂型)。其中API服务在CMO行业中占据约60%的市场份额,临床药物制造比重最小,但在创建商业制造关系中至关重要。
CMO企业专业化的技能累积往往比制药企业拥有更优质的制造能力,因此,制药企业与CMO企业合作,可以通过合成设计、工艺优化等实现药物高标准、高效率、低成本生产。 据ChemicalWeekly估计,生产环节所用成本约占新药研发总成本的30%,企业选择CMO服务,可以使生产成本下降40%-60%,即新药研发总成本下降15%左右。 随着新修订的《药品管理法》明确将在12月1日起正式实施,药品上市许可持有人制度(MAH)作为新版药品管理法的主线,我们有理由相信,国内CRO、CMO行业将迎爆发增长。笔者了解到,10月10-12日将在南昌绿地国际博览中心举办的第83届API China期间,将举办“MAH机遇与挑战论坛暨产业链创新合作模式探讨”专题论坛,吸引来自药明康德、凯莱英、华威医药、药明生物、美迪西、昭衍新药、药石科技、睿智化学等近300余家国内优秀的CRO、CMO企业参会。 *部分参展83届API China的CRO企业名单: 展商名称 展位号 爱斯特(成都)生物制药股份有限公司 A7F65 安礼特(上海)医药科技有限公司 A6C05 北京安森博医药科技有限公司 A7D80 北京海步医药科技股份有限公司北京海美桐医药科技有限公司 A6H75 北京世纪迈劲生物科技有限公司 A5F18B 沧州维智达美制药有限公司 A6H27 成都新恒创药业有限公司 A5F18C 广东利玮医药有限公司 A6H80 广州佰瑞医药有限公司 A6C07 广州隽沐生物科技股份有限公司 A5F18D 广州市桐晖药业有限公司 A7G80 广州怡正药业有限公司 A7D80-a 海门慧聚药业有限公司 A6A35 济南宝兆医药科技有限公司 A6J41 江苏先声药业有限公司 A7D89 科兴生物制药股份有限公司 A7H37 南京贝杰医药科技有限公司 A7C31 南京正济医药研究有限公司 A7G25 浦拉司科技(上海)有限责任公司 A5F18F 普洛药业股份有限公司 A6F12 山东铂源药业有限公司 A5F18G 山东中科泰斗化学有限公司 A7K03 上海力田化学品有限公司 A5F18H 苏州天马医药集团天吉生物制药有限公司 A5F18J 天津科洛医药科技有限公司 A5F18K 天津市捷安凯医药有限公司 A6C35 天津药物研究院药业有限责任公司 A6G12 亚宝药业集团股份有限公司 A5D25 浙江朗华制药有限公司 A6D18 浙江永太科技股份有限公司 A6D51 中孚药业股份有限公司 A7K15 目前参会预登记现已开通,扫码完成参会注册,赢惊喜好礼! 参会预登记现已开通 赢惊喜好礼!!! 目前100000+人已关注加入我们 点击“阅读原文”打开完成参会注册,赢惊喜好礼!返回搜狐,查看更多 |
【本文地址】
今日新闻 |
推荐新闻 |